Ботулинический токсин – актуальные вопросы применения
В 1817 г. J. Kerner впервые опубликовал описание клинических симптомов заболевания, проявляющегося мышечной слабостью вплоть до мышечного паралича, часто приводящей к смерти в результате паралича дыхательных мышц. Это заболевание назвали «ботулизм», так как им чаще страдали люди, употреблявшие в пищу колбасу без термической обработки, либо с истекшим сроком годности (от латинского botulus – колбаса).
И лишь в 1946 г. американский ученый Edward Schantz выделил и получил в чистом виде ботулинический токсин, который и вызывал это страшное заболевание. В 1977 г. офтальмолог Alan Scott сделал инъекцию ботулинического токсина первому пациенту с косоглазием и получил впечатляющий результат. Далее попытки применения ботулинического токсина привели к лечению еще одной проблемы глаза – блефароспазма, здесь также был получен положительный результат после инъекции ботулотоксина. Так началась эра применения ботулинического токсина в медицине и сейчас, наверное, нет медицинской области, где бы не использовался ботулотоксин, этот сильнейший в природе яд, но и одно из безопасных и мощных лекарств для решения проблем гиперактивности парасимпатической нервной системы.
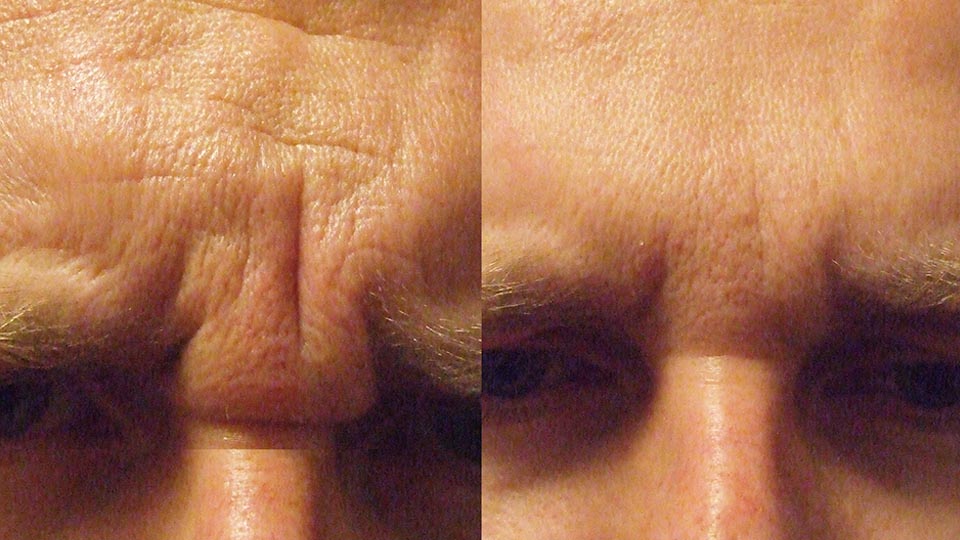
Ботулотоксин в эстетической медицине применяется с конца 80-х гг., а официальное признание метода пришло в 2000-х. Сейчас ботулотоксин является методом выбора при коррекции линий мимической экспрессии. Он является надежным, безопасным, регулируемым и обратимым методом терапии таких изменений. Кроме этого, действие ботулотоксина и его роль в предупреждении развития мимических морщин неоспорима.

Строение ботулинического токсина
Схема строения ботулинического токсина
Механизм действия ботулотоксина и его клинический эффект проявляется в виде мышечной релаксации и возможности коррекции нарушений тонуса мышц и движений. Однако терапевтическое действие токсина обратимо. Трансмиссия АЦХ восстанавливается путем реиннервации (спраутинга) нервных терминалей и формирования новых синаптических контактов, что обычно происходит в течение 3-4 месяцев и вновь обеспечивает иннервацию расслабленной мышцы.
Современное применение ботулотоксина движется в нескольких направлениях. Прежде всего более глубокое исследование и понимание механизм действия ботулинического токсина, путей и способов его распространения, отработка и уточнение мест введения, дозировок, расширение показаний, определение роли ботулотоксина в комплексной программе воздействия на возрастные изменения. Побочные эффекты после ботулотоксина, механизмы снижения и нивелирования таковых, оценка изменений психологического состояния пациента после применения препарата – все это в фокусе исследований.
Исследования показали, что после воздействия на периферические структуры нервно-мышечной проводимости возникают опосредованные изменения в вышележащих структурах нервной системы, выявлено влияние токсина на некоторые другие нейромедиаторы, кроме ацетилхолина (глутамат, субстанция Р), что объясняет анальгетический эффект применения ботулотоксина, показано поведение комплекса ботулинического токсина при попадании в мышечную ткань, уточняются механизмы формирования иммунорезистентности, сравниваются различные препараты ботулотоксинов.
Для практического врача уточняются дозировки, схема введения ботулотоксина. Тенденция применения складывается из уменьшения дозировок на точку введения, расширения мышц-мишеней, учета взаимодействия мышц на лице, разработки приемов наиболее подходящей коррекции для конкретного пациента. Исследования показали место и время введение ботулинического токсина в схемах комплексной реабилитации лица, наиболее оптимальным представляется применение ботулотоксина с препаратами контурной пластики.
Токсин при внутримышечных инъекциях
Так, Hallett M. (2015)в системном обзоре показывает некоторые особенности поведения ботулотоксина в организме: токсин, который не захватился аксоном, попадает в системный кровоток, где его поведение и период полураспада неизвестен (в экспериментальных моделях около 230 мин). Предположительно он метаболизируется и выводится печенью.
Прикрепление токсина зависит от мышечной активности и температуры. Чем выше мышечная активность, тем больше молекул прикрепляется на аксон, охлаждение же места инъекции ведет к торможению этих процессов. Время нахождения во внеклеточном пространстве точно не определено, но исследование показало, что полупериод захвата составляет около 12 минут. Время внедрения в аксон составляет около 30 мин. Время от инъекции до расслабления определяется длительностью достаточного повреждения транспортной системы (в экспериментальных моделях около 90 мин). Токсин вероятно метаболизируется, в основном, протеасомным путем (убиквитин – зависимая деградация), и это занимает несколько месяцев.
Исследования последних лет свидетельствуют о способности ботулотоксина ингибировать высвобождение глютамата, связанного с геном кальцитонина, а также медиатора воспаления субстанции Р, что позволяет более обоснованно применять токсин в лечении болевых синдромов. Уже показано действие ботулотоксина на различные нейромедиаторные системы.
Краткий обзор приведен в таблице 1.
|
Нейротрансмиттеры |
Материал исследования |
Авторы |
|
Ацетилхолин
|
Нейромышечный синапс; Электрический орган ската; Аплазия ЦНС |
Burgen et аl., 1949; Dunant et al.,1987; Poulain et al., 1988 |
|
Глутамат
|
Синаптосомы мозга; Масс-спектрометрия крысиной лапки |
Sanchez Prieto et al., 1987; Cui et al., 2004 |
|
Аспартат |
Синаптосомы мозга |
McMahon et al., 1992 |
|
ГАМК |
Синаптосомы мозга |
Ashton et al., 1988; McMahon et al., 1992; Neales et al., 1999 |
|
Глицин |
Первичная культура нейронов спинного мозга |
Maisey et al., 1988; Ashton et al., 1988 |
|
Дофамин, адреналин, НА |
Синаптосомы мозга |
Najib et al., 1999 |
|
Серотонин |
Синаптосомы мозга |
Marsal et al., 1990 |
|
АТФ (выброс с АЦХ) |
Синаптосомы мозга |
Hassan et al., 1994; Meunier et al., 1996 |
|
Кальцитонин-гензависимый пептид |
Нейромышечный синапс (аккумуляция); Аксоны тройничного нерва |
Durham et al., 2004 |
|
Субстанция Р
|
Нейроны межпозвоночных ганглиев |
Purkiss et al., 1997; Welch et al., 2000 |
Иммунорезистентность токсина
Для INCO ботулинотоксина (препарат Xeomin) – 0,8-1,1%, для ABO ботулинотоксина (препарат Dysport) –1,4%, для ONA (препарат Botox – 3,6%).
Исследователи сделали выводы, что общее количество случаев образования антител было невелико, одинаково для ABO и INCO, и достоверно выше для ONA. В эстетической медицине вопрос образования антител очень дискутабелен, так как применяемые дозы невелики и сколько-нибудь значимых наблюдений возникновения нечувствительности нет.
Важным представляется вопрос безопасности длительного применения ботулотоксина при различных патологиях. В нашей практике есть пациенты, получившие более 40 циклов терапии токсином. Мы не видели значимых побочных эффектов, также не было причин для прерывания терапии. Многочисленные исследования также подтверждают высокую безопасность ботулотоксина.
Так длительное применение ботулотоксина (Ботокс, Ксеомин, Диспорт) при лечении блефароспазма (K. Kollewe et al., 2015) у 208 больных, 11,2+/-4,1 лет наблюдения, 10 701 сеансов показало высокий терапевтический эффект, без каких-либо стойких побочных эффектов. Показано, что применение ботулинотерапии до и во время беременности не влияет на развитие плода (дефекты развития плода у группы наблюдения сопоставимы со средними в популяции) (M. Brin et al., 2015). Длительное применение ботулинотерапии (от 10 до 26 лет) при лечении дистоний показывает ее эффективность и безопасность. При этом не отмечается существенных вариаций в эффективности, длительности и изменении дозы препарата (J. Jankovic, 2015). Длительное применение препаратов ботулотоксина в эстетической медицине также показало ее эффективность и стабильный результат в течение длительного времени (от 6 до 17 лет), в сочетании с контурной пластикой и другими косметологическими процедурами (A.Carruthers et al., 2015).
В заключение
Наука о ботулинотерапии развивается семимильными шагами. Поскольку токсин ботулизма является биологически продуцируемым протеином, молекула его обладает специфическими участками, ответственными за его эффект (способность к специфическому связыванию с внеклеточными структурами и внутриклеточными ферментами). Токсин обладает огромным потенциалом при его использовании в области белковой инженерии с созданием новых биологически активных молекул, обладающих новыми свойствами. Уже сделаны первые шаги в попытке создать методом белковой инженерии молекулы-гибриды, состоящие из молекул токсина ботулизма типа А и столбнячного токсина. Основной целью является создание молекул, обладающих специфической активностью по отношению к различным клеткам и типам тканей. Это откроет большие возможности лечения многих типов заболеваний, лежащих за рамками нервно-мышечных расстройств.
Несмотря на столь бурное развитие знаний о ботулотоксине до сих пор многие вопросы, касающиеся применения токсина ботулизма, остаются без ответа. Многие вопросы не ясны даже относительно уже традиционных аспектов применения токсина (механизмы транспорта токсина, иммунные реакции и образование антител, гетерогенность клинических результатов), разная длительность и выраженность положительного эффекта, роль других серотипов токсина. Большая ниша, связанная с генетикой, требует дальнейшей разработки. Поэтому и ученым и врачам практикам еще предстоит сделать много, чтобы ответить на все эти вопросы, существует огромный потенциал для разработки новых показаний к применению токсина, созданию новых производных токсина и пониманию глубинных механизмов действия.
Сергей Шелехов, к. м. н., невролог, член экспертного совета по ботулинотерапии стран СНГ, Алматы, журнал Beauty Code, 2015/4